尊龙凯时产品性能对比分析
背景
纵观生物药物生产的历程,有效地去除和检测宿主细胞蛋白(HCP)杂质的研究和发现层出不穷。这些杂质的存在对临床病人的安全以及药物的稳定性产生了重要影响。
表达系统概述
在当前的蛋白药物表达系统中,主要分为原核表达系统(如大肠杆菌E. coli)、植物表达系统、真菌表达系统(如毕赤酵母、酿酒酵母)、昆虫表达系统(如S. frugiperda和SF9细胞)、以及哺乳动物细胞表达系统(如中国仓鼠卵巢细胞CHO和非洲绿猴肾细胞Vero等)。其中,哺乳动物细胞系统广泛应用于临床药物生产,但成本较高;而E. coli表达系统因其产量高、成本低,被广泛采用。
E. coli表达系统特点
E. coli表达系统是应用最广泛的表达系统之一,因其培养简单、转化效率高和成本低而受到青睐。例如,不需要糖基化修饰的人胰岛素和生长激素,仍具生物学活性。此外,虽然一些蛋白质在自然状态下需要糖基化修饰,但在E. coli系统中也可被有效表达。
HCP检测方法
目前,HCP的检测和鉴定方法主要有ELISA和LC-MS,其中ELISA在高通量定量方面具有优势且成本低廉,而LC-MS则提供定量与定性支持,但价格较高且通量较低。通常需要将两者结合使用,以便更全面地定性和定量药物中的HCP。
HCP差异性分析
不同药物相同纯化工艺或相同药物不同工艺的HCP残留差异显著,因此,国内外的药物HCP定量结果差异明显。E. coli HCP与CHO HCP之间存在较大差别,通常可分为以下几类:
- 黏附素:如Curli(CsgA),形成淀粉样纤维,促进生物膜形成;
- 毒素:如α-溶血素(HlyA),溶解红细胞和上皮细胞;
- 侵袭素:如OmpA,促进E. coli侵袭血脑屏障;
- 免疫逃逸相关蛋白:如LPS,诱导炎症但逃避免疫识别;
- 分泌系统效应蛋白:如EspC,自转运蛋白酶破坏上皮屏障;
- 宿主互作效应蛋白:如NleH,干扰NF-κB通路减少炎症;
- 致病基因:如Colibactin,诱导DNA损伤。
HCP检测的重要性
研究表明,残留的HCP可能导致免疫原性与药物辅料的降解。因此,对宿主细胞的高风险因子进行基因敲除或使用空载HCP模拟药物生产及纯化过程中的残留分析显得尤为重要。在药物优化和纯化过程中,有些HCP难以清除。例如,E. coli表达的 malaria vaccine 在纯化过程中HCP含量范围在90 ng/g至1100 ppm/剂之间,但临床上可接受的HCP含量仅为<100 ppm/剂。
尊龙凯时的产品检测结果
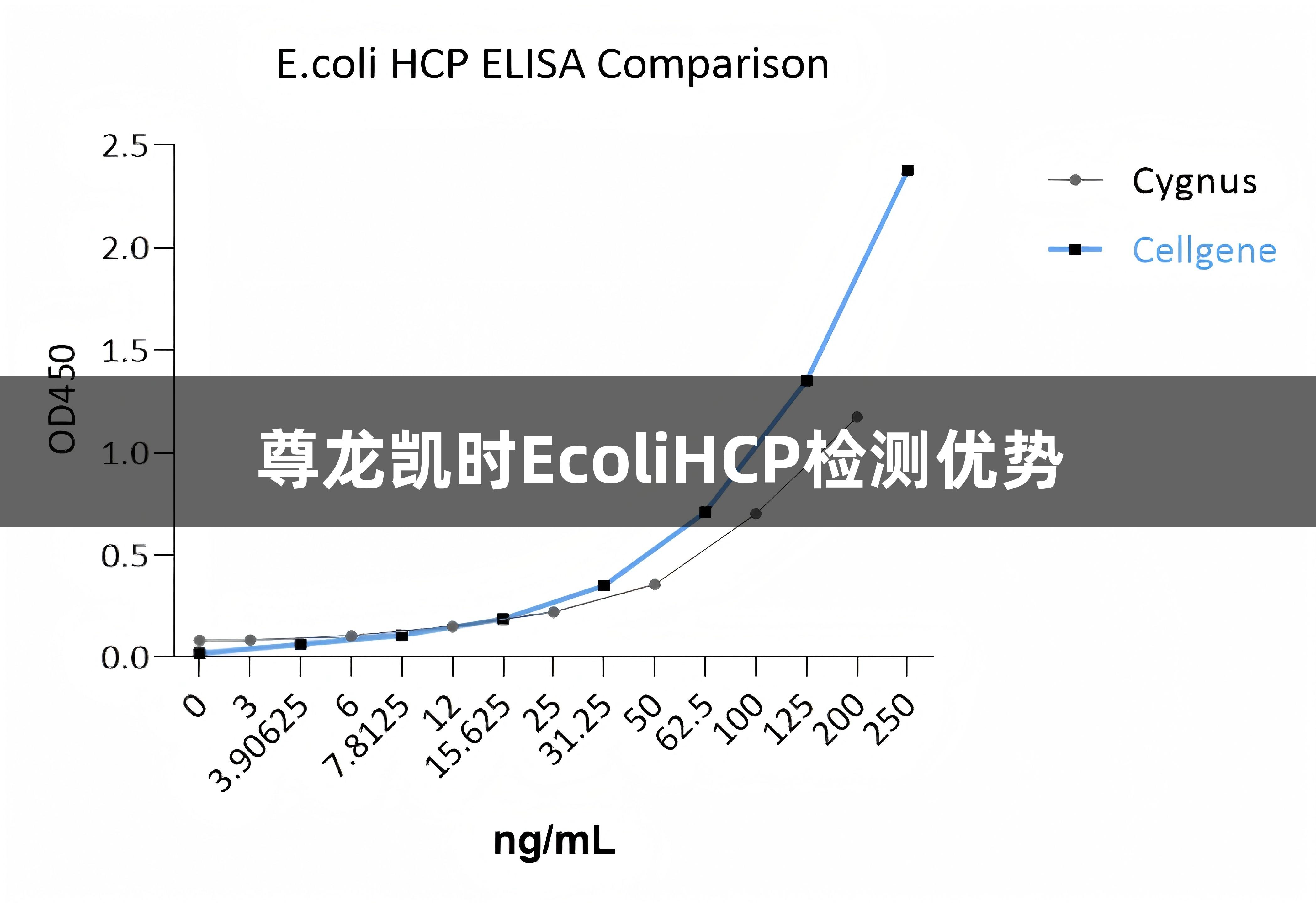
尊龙凯时新开发的E. coli HCP (6S) ELISA/EH-E0022-3与美国Cygnus/F410产品进行了比较,主要从标曲范围、样本相对变化率、样本检测浓度和本底四个方面进行了分析。结果表明:
- 本底相对更低,能排除更多非特异性结合;
- 样本相对变化率更稳定,检测区间广泛;
- 样本检测浓度显著更高。
结论
针对HCP的检测,尊龙凯时始终致力于提高检测的灵敏度与覆盖度,推动生物药物生产的技术进步,确保药物的安全性和有效性。


